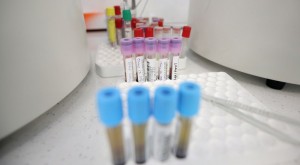
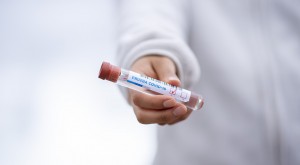
Испанската агенция по лекарства (AEMPS) разреши клиничното изпитване на ваксината PHH-1V срещу COVID-19, разработена от испанската компания Hipra.
Новината дойде няколко дни след като същата агенция отказа клинични проучвания при хора на друга испанска ваксина, разработена от екипа на Мариано Естебан от Висшия съвет за научни изследвания (CSIC), съвместно с фармацевтичната компания Biofabri.
Одобреното изпитване е за първа фаза и ще изследва преди всичко безопасността и поносимостта на ваксината, както и нейната ефикасност. За тази цел ще бъдат наети няколко десетки доброволци на възраст между 18 и 39 години.
Всеки от тях ще получи две дози с интервал от 21 дни. Ако всичко върви добре и клиничните изпитвания са успешни, компанията да започне производството още през октомври тази година. През следващата година година се очаква да бъдат произведени 400 млн. дози, а през 2023 г. да достигнат 1,2 млрд., предаде БНР.
Заради факта, че ще се съхранява при температура между 2 и 8 ºC се очаква и разпространението й да е по-лесно. Премиерът Педро Санчес обяви, че правителството е предоставило 13 млн. евро за разработването на ваксината, а министърът на науката и иновациите Диана Морант уточни, че тя е "много важна стъпка за испанската наука", защото ще е ефективна и срещу новите мутации на коронавируса.
Това се случи Dnes, за важното през деня ни последвайте и в Google News Showcase





 Хартиените ваучери за храна остават в миналото. Ще "изгорят" ли парите от тях?
Хартиените ваучери за храна остават в миналото. Ще "изгорят" ли парите от тях?  Васил Терзиев: Дано след изборите да има стабилност, от липсата й губим всички
Васил Терзиев: Дано след изборите да има стабилност, от липсата й губим всички  Бизнесът и политиката трябва да се срещнат, за да не ни третират като второ качество хора
Бизнесът и политиката трябва да се срещнат, за да не ни третират като второ качество хора  В Пловдив забраниха алкохола в изборния ден
В Пловдив забраниха алкохола в изборния ден 
 Как изкуственият интелект може да открие деменция с телца на Леви въз основа на речта?
Как изкуственият интелект може да открие деменция с телца на Леви въз основа на речта?  В България липсва комплексност при лечението на рак на гърдата
В България липсва комплексност при лечението на рак на гърдата  Хемороиди - обострят се през преходните сезони?
Хемороиди - обострят се през преходните сезони?  Бягане или ходене по наклон - кое изгаря повече мазнини?
Бягане или ходене по наклон - кое изгаря повече мазнини? 
 Подсигурете си успеха в света на технологиите, момичета
Подсигурете си успеха в света на технологиите, момичета  Любовен хороскоп за лято 2024
Любовен хороскоп за лято 2024  Кайли Дженър и Тимъти Шаламе са много щастливи заедно
Кайли Дженър и Тимъти Шаламе са много щастливи заедно  6 тенденции в банските за лятото
6 тенденции в банските за лятото 
 Акция на седмицата: "Дронамикс Кепитъл" АД
Акция на седмицата: "Дронамикс Кепитъл" АД  В средата на епичната година на избори изводът е очаквайте неочакваното
В средата на епичната година на избори изводът е очаквайте неочакваното  "Роснефт": "Фантомни барели" доведоха до спад на цената на петрола
"Роснефт": "Фантомни барели" доведоха до спад на цената на петрола  Оман е новата "гореща точка" за търговията с Русия в Персийския залив
Оман е новата "гореща точка" за търговията с Русия в Персийския залив 
Коментари Напиши коментар